Biologie cellulaire : Méthodes d’études cellulaires
I) Les méthodes d’observation
1) Méthodes et techniques d’observations des cellules
1) Méthodes et techniques d’observations des cellules
L’observation des cellules est délicate du fait de leurs très petites tailles, et nécessite un certain nombre d’appareillages dont les microscopes. On distingue deux grands types de microscopes suivant leur résolution : les microscopes optiques et les microscopes électroniques
a) Microscopes optiques
Les microscopes optiques (à lumière ou photoniques) permettent l’observation de cellules vivantes ou mortes, grâce à des coupes très fines de préparations fixées. Les microscopes optiques utilisent de la lumière visible et la qualité de l’image dépend du pouvoir séparateur qui donne la résolution du microscope limitée par la longueur d’onde de la radiation lumineuse. On obtient donc un grossissement x1000
Pour les microscopes optiques à fluorescence la lumière reçue par l’œil ne traverse pas l’objet ; ici on utilise des molécules fluorescentes appelées des fluorochromes, qui sont utilisés comme colorant. La lumière excite les fluorochromes qui réémettent dans des plus grandes longueurs d’ondes c’est-à-dire dans des énergies plus basses
Dans ce type de microscope on utilise des filtres qui permettent la formation d’une lumière monochromatique qui éclairera l’échantillon (cf. cours de physique). Les microscopes optiques à fluorescence nécessitent des cellules fixées, des coupes minces et entraînent malheureusement des superpositions d’images
Les microscopes optiques à fluorescence sont souvent équipés de microscopie confocale qui remédie à la superposition d’images, en étudiant la cellule plan par plan
b) Microscopes électroniques
Les microscopes électroniques utilisent des faisceaux d’électrons qui sont chargés, possèdent une masse et se comportent comme une onde. Plus les électrons sont accélérés plus les longueurs d’onde diminuent et plus la résolution augmente. Ces électrons possèdent des compartiments possédant un vide parfait afin de maintenir rectiligne les faisceaux d’électrons, et des lentilles électromagnétiques qui forment un condensateur. On obtient ici un grossissement x 100 000. Les microscopes électroniques nécessitent la déshydratation de l’échantillon et donc la mort des cellules et du fait du faible pouvoir pénétrant des électrons les échantillons doivent être sous forme de coupes ultra fines et donc soumis à des inclusions
La microscopie électronique à balayage consiste à balayer une préparation par un faisceau d’électrons, permettant la mise en évidence des reliefs de l’échantillon
2) Techniques de préparation des échantillons
a) Etudes des structures
a) Etudes des structures
Afin d’étudier des structures on utilise un certain nombre de techniques : préparation des coupes fines, coloration négative, ombrage métallique, cryodécapage
La préparation des coupes fines se fait en plusieurs étapes
La fixation se fait par le formaldéhyde et le glutaraldéhyde, qui sont des aldéhydes très réactifs. Malheureusement la fixation tue les cellules mais permet leur immobilisation et leur conservation
La déshydratation permet l’élimination de l’eau en la remplaçant par des solvants de types xylène et toluène
L’inclusion dans de la résine, cire ou paraffine, permet une solidification de l’échantillon, par leur polymérisation
La formation des coupes ultrafines est réalisée par des microtomes
La coloration des coupes se fait par différents types de colorants ou méthodes de mise en évidence
Les colorants métachromatiques qui changent de couleur suivant la nature des structures colorées. On donnera comme exemple le May-Grunwald-Giemsa (MGG), qui correspond à l’association d’éosine et de bleu de méthylène, permettant la coloration des frottis sanguins
Les colorants histochimiques comme l’acide périodique de Schiff qui colore les polysaccharides et le noir soudan qui colore les lipides
La méthode histo-enzymatique qui permet la formation d’un produit coloré par action d’une enzyme sur son substrat incolore
Le montage rend la préparation observable
La coloration négative permet de mettre en évidence le contour de petits objets, grâce à des projections de métaux lourds sur la préparation
La déshydratation permet l’élimination de l’eau en la remplaçant par des solvants de types xylène et toluène
L’inclusion dans de la résine, cire ou paraffine, permet une solidification de l’échantillon, par leur polymérisation
La formation des coupes ultrafines est réalisée par des microtomes
La coloration des coupes se fait par différents types de colorants ou méthodes de mise en évidence
Les colorants métachromatiques qui changent de couleur suivant la nature des structures colorées. On donnera comme exemple le May-Grunwald-Giemsa (MGG), qui correspond à l’association d’éosine et de bleu de méthylène, permettant la coloration des frottis sanguins
Les colorants histochimiques comme l’acide périodique de Schiff qui colore les polysaccharides et le noir soudan qui colore les lipides
La méthode histo-enzymatique qui permet la formation d’un produit coloré par action d’une enzyme sur son substrat incolore
Le montage rend la préparation observable
La coloration négative permet de mettre en évidence le contour de petits objets, grâce à des projections de métaux lourds sur la préparation
Les ombrages métalliques permettent d’accentuer les reliefs d’un objet en vaporisant sous vide une très fine couche métallique avec un certain angle d’incidence entraînant la formation d’ombre portée
b) Mise en culture
La culture cellulaire est obtenue après le maintien en vie de cellules plus de 24 heures dans un milieu de culture artificielle. On met en évidence deux types de cultures
Les cultures organotypiques sont soumises à un maintien de la différentiation morphologique et fonctionnelle. Ces fragments d’organes ou tissus sont appelés des explants
Les cultures histiotypiques correspondent à une multiplication active mais sans maintien de l’organisation
Les cultures histiotypiques correspondent à une multiplication active mais sans maintien de l’organisation
II) Les méthodes de fractionnement subcellulaire
Les méthodes de fractionnement subcellulaire consistent à séparer les différents composants cellulaires par destruction de la membrane plasmique, puis par désorganisation de la cellule
Les méthodes de fractionnement subcellulaire consistent à séparer les différents composants cellulaires par destruction de la membrane plasmique, puis par désorganisation de la cellule
1) Homogénéisation
Le but de l’homogénéisation est de rompre la membrane plasmique (ou la paroi pour les cellules végétales et fongique). Pour se faire on met les cellules en suspension dans un tampon de pH et de force ionique connus
L’homogénéiseur est un tube de verre dans lequel on place la préparation puis un piston en verre. La cellule passera entre le tube de verre et le piston, sera ainsi comprimée et éclatera, libérant son contenu dans le tampon
On obtient un homogénat avec tous les constituants de la cellule. La plupart des organites restent intactes, mais sans précaution particulière l’appareil de Golgi et le réticulum endoplasmique vont être fragmentés sous forme de vésicules appelées microsomes
2) Purification
a) Centrifugation différentielle
La centrifugation différentielle permet la purification de l’homogénat en fonction de la taille et de la densité de ses constituants. Pour se faire on centrifuge l’homogénat à différentes vitesses ; à chaque vitesse, différents organites se déposent dans le culot, qui sera prélevé
A 600g, on observe la sédimentation du noyau et du cytosquelette
A 15 000g, on observe la sédimentation des mitochondries, des lysosomes et des peroxysomes
A 100 000g (ultracentrifugation), on observe la sédimentation de la membrane plasmique, des microsomes et des grands polysomes
A 200 000g, on observe la sédimentation des ribosomes et des petits polysomes. Ce qui reste à la fin c’est la fraction hydrosoluble du cytosol
b) Centrifugation par gradient préformé
A 15 000g, on observe la sédimentation des mitochondries, des lysosomes et des peroxysomes
A 100 000g (ultracentrifugation), on observe la sédimentation de la membrane plasmique, des microsomes et des grands polysomes
A 200 000g, on observe la sédimentation des ribosomes et des petits polysomes. Ce qui reste à la fin c’est la fraction hydrosoluble du cytosol
b) Centrifugation par gradient préformé
La centrifugation par gradient préformé consiste à déposer une mince couche d’homogénat au dessus de la solution de saccharose dont la concentration varie de façon régulière et décroissante du bas vers le haut. Les différents constituants de l’homogénat sédimentent tous à des vitesses différentes, on obtient ainsi différentes bandes (la couche la plus dense étant au fond) que l’on séparera
La vitesse de sédimentation dépend de la taille des molécules, de la forme des particules et de la densité. La vitesse de sédimentation est définie par le coefficient de sédimentation en unité Svedberg (S
Biologie cellulaire : membranes cellulaires
DÉFINITION:
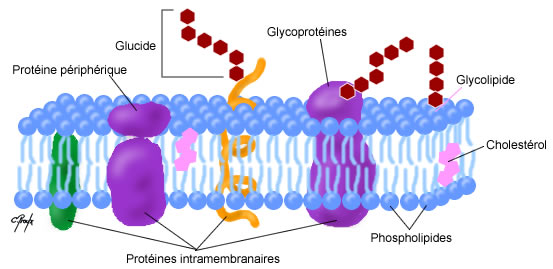
Les membranes cellulaires sont des doubles couches phospholipidiques dans lesquelles s’insèrent de manière asymétrique et inhomogène d’autres structures les caractérisant
Les membranes cellulaires sont des doubles couches phospholipidiques dans lesquelles s’insèrent de manière asymétrique et inhomogène d’autres structures les caractérisant
La membrane délimitant la cellule est appelée membrane plasmique et les membranes des organites sont appelées par le nom de l’organite concerné (membrane nucléaire, membrane mitochondriale, etc
En microscopie électronique on observe une tri-lamination de la membrane : un feuillet clair de 3 nm (environ 2 fois la longueur d’une chaîne d’acide gras) entouré par 2 feuillets sombres de 2,5 nm chacun ; l’épaisseur totale est donc d’environ 8 nm. Ceci a permis de mettre en évidence la structure en bicouche phospholipidique de la membrane plasmique
I) Composition des membranes
Les membranes sont constituées (en poids sec de membrane) de 40% de lipides, 52% de protéines et 8% de glucides. En prenant en compte la différence de poids existant entre ces classes de molécules, on compte 50 molécules de lipides par molécule de protéine
Les membranes sont constituées (en poids sec de membrane) de 40% de lipides, 52% de protéines et 8% de glucides. En prenant en compte la différence de poids existant entre ces classes de molécules, on compte 50 molécules de lipides par molécule de protéine
1) Diversités des lipides membranaires
Au sein de la membrane les lipides sont présents sous différentes formes ; parmi elles on compte les phospholipides, les glycolipides et le cholestérol
a) Phospholipides
Les phospholipides présentent tous une tête hydrophile (phosphate et groupement spécialisé) et une queue hydrophobe (glycérol et acides gras). On distingue deux types de phospholipides
Les glycérophospholipides correspondent à l’association de glycérol, de deux acides gras, d’un acide phosphorique et d’alcools ou d’acides aminés (cf. cours de biochimie). Les alcools ou les acides aminés donnent l’identité et la caractéristique du glycérophospholipides. Parmi les acides aminés on trouve la sérine et parmi les alcools on trouve l’inositol, l’éthanolamine et la choline ; on obtient ainsi la phosphatidyl-sérine, le phosphatidyl-inositol, la phosphatidyl-éthanolamine et la phosphatidyl-choline
Les sphingophospholipides correspondent à l’association de sphingosine, d’acide gras, d’acide phosphorique et d’alcool ou d’acides aminés ; on obtient ainsi la sphingomyéline (par association de la choline
Les sphingophospholipides correspondent à l’association de sphingosine, d’acide gras, d’acide phosphorique et d’alcool ou d’acides aminés ; on obtient ainsi la sphingomyéline (par association de la choline
b) Glycolipides
Les glycolipides sont de deux types, on trouve les glycéroglycolipides et les sphingoglycolipides. Il est intéressant de préciser que les glycolipides des membranes des érythrocytes (globules-rouges), définissent le groupe sanguin de l’individu
c) Cholestérol
Le cholestérol est uniquement présent dans les membranes des cellules animales, en effet, il est absent des cellules végétales et des bactéries. Le cholestérol est composé d’un noyau stéroïde hydrophobe, d’une queue hydrophobe et d’une fonction alcool hydrophile. La molécule est donc amphiphile, représente environ un quart des lipides membranaires et influence la fluidité membranaire (cf. cours de biochimie
2) Diversités des protéines membranaires
Les protéines membranaires ont des rôles bien spécifiques au sein de la double couche phospholipidique : récepteurs, transporteurs, adhérence cellulaire, catalyse enzymatique, messagers intracellulaires, etc. Chaque protéine possède une extrémité N-terminale et une extrémité C-terminale (cf. cours de biologie moléculaire – Traduction). Les protéines sont ancrées de différentes manières dans la membrane
a) Les protéines extrinsèques
Les protéines extrinsèques sont localisées en dehors de la bicouche phospholipidique et sont ainsi soit entièrement intracellulaire, soit entièrement extracellulaire. Elles interagissent avec la membrane, par des liaisons électrostatiques de types liaisons hydrogènes et liaisons de Van der Waals, au niveau de domaines caractéristiques de protéines transmembranaires ou de lipides. Ces interactions étant faibles, elles sont rompues facilement par des variations de forces ioniques et de pH
b) Les protéines ancrées dans des acides gras
Les protéines périphériques ancrées dans les lipides sont de deux types
Ancrées sur les glyco-phosphatidyl-inositol (GPI) qui correspondent à l’association d’une phospho-éthanol-amine sur des sucres, eux-mêmes ancrés sur un phosphatidyl-inositol. Ces protéines sont présentent sur la face extracellulaire de la membrane
Ancrées à la membrane par l’intermédiaire d’acide gras (acide palmitique et acide myristique). Ces protéines sont présentent sur la face intracellulaire de la membrane
c) Les protéines transmembranaires
Ancrées à la membrane par l’intermédiaire d’acide gras (acide palmitique et acide myristique). Ces protéines sont présentent sur la face intracellulaire de la membrane
c) Les protéines transmembranaires
Les protéines transmembranaires traversent les deux feuillets de la membrane. Ces protéines sont liées de manière stable à la membrane avec l’environnement hydrophobe de la face interne de la membrane, par les acides aminés apolaires de leurs hélices α. Elles ne peuvent ainsi être séparées de la double couche phospholipidique (et donc étudiées) que par l’action de détergents
3) Diversités des glucides membranaires
La grande majorité des glucides membranaires sont sous forme de glycoprotéines et une petite partie sous forme de glycolipides. Au niveau de la membrane les glucides n’existent pas à l’état libre, ils sont liés à des protéines, par des liaisons N-glycosidiques (le plus souvent) et des liaisons O-glycosidiques, sous forme de petites glycoprotéines ou de protéoglycanes
Les glycoprotéines contiennent des polysaccharides courts, souvent ramifiés et n’excédant pas 50% du poids moléculaire de la glycoprotéine. Le sucre terminal est souvent de l’acide sialique chargé négativement
Les protéoglycanes sont également des glycoprotéines, mais qui contiennent des polysaccharides à chaîne longue composée d’unités disaccharidiques répétées à l’infini, représentant jusqu’à 90% du poids moléculaire globale. Souvent un des deux sucres de l’unité est aminé, on parle alors de glyco-amino-glycane (ou GAG) dont le plus simple est l’acide hyaluronique
Pour information, les protéoglycanes sécrétoires composent la matrice extracellulaire (tissu conjonctif, cartilage, etc.) et sont différents des protéoglycanes cellulaire
Les protéoglycanes sont également des glycoprotéines, mais qui contiennent des polysaccharides à chaîne longue composée d’unités disaccharidiques répétées à l’infini, représentant jusqu’à 90% du poids moléculaire globale. Souvent un des deux sucres de l’unité est aminé, on parle alors de glyco-amino-glycane (ou GAG) dont le plus simple est l’acide hyaluronique
Pour information, les protéoglycanes sécrétoires composent la matrice extracellulaire (tissu conjonctif, cartilage, etc.) et sont différents des protéoglycanes cellulaire
II) Propriétés des membranes
1) Auto-assemblage des lipides
1) Auto-assemblage des lipides
Les phospholipides, dus à leurs propriétés physico-chimiques, s’assemblent de manière automatique en différentes sortes de structures suivant l’environnement
Les monocouches sont des couches mono-moléculaires dont les têtes hydrophiles sont dirigées vers le milieu aqueux et les queues hydrophobes vers le milieu lipidiques
Les micelles sont des formations sous la forme de gouttelettes rondes, où dans un milieu aqueux les têtes hydrophiles sont dirigées vers l’extérieur de la sphère et les queues hydrophobes sont dirigées vers l’intérieur (dans un milieu lipidique la conformation est inverse
Les bicouches phospholipidiques permettent la formation de vésicules sphériques appelées liposomes. Les bicouches phospholipides rentrent dans la formation des bicouches membranaires. Pour information, les liposomes sont actuellement utilisés en thérapeutique pour encapsuler des substances médicamenteuses
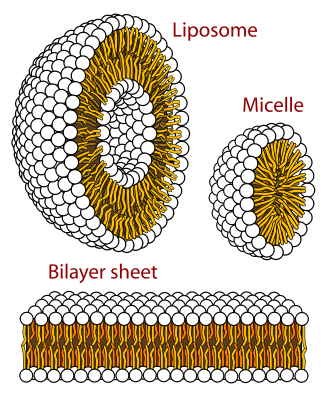
Les micelles sont des formations sous la forme de gouttelettes rondes, où dans un milieu aqueux les têtes hydrophiles sont dirigées vers l’extérieur de la sphère et les queues hydrophobes sont dirigées vers l’intérieur (dans un milieu lipidique la conformation est inverse
Les bicouches phospholipidiques permettent la formation de vésicules sphériques appelées liposomes. Les bicouches phospholipides rentrent dans la formation des bicouches membranaires. Pour information, les liposomes sont actuellement utilisés en thérapeutique pour encapsuler des substances médicamenteuses

2) Asymétrie membranaire
Toutes les membranes biologiques sont constituées de feuillets dont les compositions lipidiques sont différentes, sauf le cholestérol qui se trouve en quantité équivalente dans l’un ou l’autre des feuillets, pouvant basculer facilement de l’un à l’autre
Le feuillet interne est caractérisé par les phosphatidyl-sérine (amphotère) et phosphatidyl-éthanol-amine (charge négative
Le feuillet externe est caractérisé par la sphingomyéline (charge négative) et la phosphatidyl-choline (charge négative
L’asymétrie des lipides entraîne ainsi une asymétrie de la charge globale de chaque feuillet. On visualise également une asymétrie des protéines présente dans la double couche phospholipidique ; ces protéines participent à caractériser les propriétés de la membrane, que cela soit du côté intracellulaire ou extracellulaire
Le feuillet externe est caractérisé par la sphingomyéline (charge négative) et la phosphatidyl-choline (charge négative
L’asymétrie des lipides entraîne ainsi une asymétrie de la charge globale de chaque feuillet. On visualise également une asymétrie des protéines présente dans la double couche phospholipidique ; ces protéines participent à caractériser les propriétés de la membrane, que cela soit du côté intracellulaire ou extracellulaire
La plus grande asymétrie est celle présente au niveau des glucides, en effet tous les motifs glucidiques sont localisés sur le feuillet externe de la membrane plasmique. Pour les organites intracellulaires les sucres sont dirigés vers la lumière de l’organite. « L’arbre glucidique » présent au niveau du feuillet externe de la membrane plasmique forme ce que l’on appelle le glycocalix
3) Fluidité membranaire
La mobilité des lipides est nécessaire pour l’activité cellulaire. Ils peuvent se mouvoir de différentes manières au sein de la membrane : rotation, diffusion latéral et flip flop (passage d’un feuillet à l’autre
Certaines protéines vont être bloquées par des structures intracellulaires ou extracellulaires par des interactions protéines-protéines ou interactions avec le cytosquelette
La fluidité membranaire intervient dans différentes fonctions cellulaires : absorption, sécrétion, protection, adhérence, communication, interaction avec la matrice, etc
La fluidité est influencée par différents facteurs, des facteurs externes comme la température (une augmentation de la température entraîne la fluidification de la membrane) et des facteurs internes
Certaines protéines vont être bloquées par des structures intracellulaires ou extracellulaires par des interactions protéines-protéines ou interactions avec le cytosquelette
La fluidité membranaire intervient dans différentes fonctions cellulaires : absorption, sécrétion, protection, adhérence, communication, interaction avec la matrice, etc
La fluidité est influencée par différents facteurs, des facteurs externes comme la température (une augmentation de la température entraîne la fluidification de la membrane) et des facteurs internes
La composition en acides-gras : Plus les chaînes carbonées des acides-gras sont courtes et insaturées plus la membrane est fluide
La proportion de cholestérol : Le cholestérol renforce la solidité et rigidité membranaire et correspond jusqu’à 50% des lipides totaux de la membrane
Le nombre de protéines : Les protéines diminuent la fluidité membranaire
La proportion de cholestérol : Le cholestérol renforce la solidité et rigidité membranaire et correspond jusqu’à 50% des lipides totaux de la membrane
Le nombre de protéines : Les protéines diminuent la fluidité membranaire
III) Différenciation de la membrane plasmique
On distingue 3 principaux types de différenciation de la membrane plasmique, qui touche des pôles différents de la cellule concernée
On distingue 3 principaux types de différenciation de la membrane plasmique, qui touche des pôles différents de la cellule concernée
1) La bordure en brosse
La bordure en brosse est un rassemblement de microvillosités qui touche la membrane plasmique du pôle apical des cellules, permettant une augmentation de la surface d’échanges des cellules épithéliales (entérocytes, tubules rénaux, etc
Les microvillosités sont constituées de faisceaux de microfilaments d’actines, parallèlement par rapport à l’axe de la microvillosité. A la base de la microvillosité on trouve des filaments intermédiaires qui s’orientent de manière perpendiculaire par rapport aux microvillosités. La structure des faisceaux est permise grâce aux villines et fimbrines qui unissent les microfilaments d’actines entre eux (cf. chapitres microfilaments d’actines). Les faisceaux sont fixés à la membrane à l’aide de protéines contractiles : les myosines 1 latéralement et les myosines 5 à la pointe de la microvillosité
2) Les microvillosités isolées
Les microvillosités peuvent être distantes les unes des autres, on parle de microvillosités isolées. Ces dernières sont notamment visibles au niveau des polynucléaires (ou globules-blanc ou leucocytes) lors de la diapédèse (cf. cours d’immunologie – « Immunité innée »
3) Les intra-digitations
Les intra-digitations correspondent à des replis de la membrane plasmique au niveau du pôle basal des cellules épithéliales, le plus souvent au niveau de cellules qui sont sujettes à des échangent d’eau et de minéraux de manière bidirectionnelle avec la matrice extracellulaire
 mars 10th, 2012
mars 10th, 2012 


Aucun commentaire:
Enregistrer un commentaire